Sepsis zählt weltweit zu den häufigsten Erkrankungen und Todesursachen. 48,9 Millionen Menschen erkranken an einer Sepsis, etwa 20 Prozent aller Todesfälle sind mit der Erkrankung assoziiert, wie eine Studie des Institute for Health Metrics and Evaluation (IHME) zeigt. Auch in Deutschland gehört die Sepsis zu den häufigsten Todesursachen. An diesem Punkt setzt ein Forschungsprojekt der TU Wien in Zusammenarbeit mit der Medizinischen Universität Wien an.
Prof. Clemens Heitzinger vom Forschungsbereich maschinelles Lernen der Fakultät für Informatik und sein Team entwickelten eine künstliche Intelligenz, die Vorschläge für die Behandlung von Menschen liefert, die wegen einer Sepsis intensivmedizinische Betreuung brauchen. „Es besteht oft das Problem, dass die Sepsis nicht früh genug erkannt wird“, sagt Heitzinger. Ursprünglich aus der Mathematik kommend, beschäftigte er sich schon länger mit dem Reinforcement Learning und suchte nach sicherheitskritischen Anwendungen. Bei diesen müsse klar sein, dass die bestmögliche Lösung notwendig ist. „Wir benötigen die besten Algorithmen und müssen uns auch überlegen, wie zuverlässig die Strategien sind, die wir berechnen“, erklärt er. Dadurch kam er zur Medizin und stieß letztlich auf die Sepsis – die durch ihre Häufigkeit auch eine entsprechend große Datenlage mit sich bringt.
200 Vitalparameter

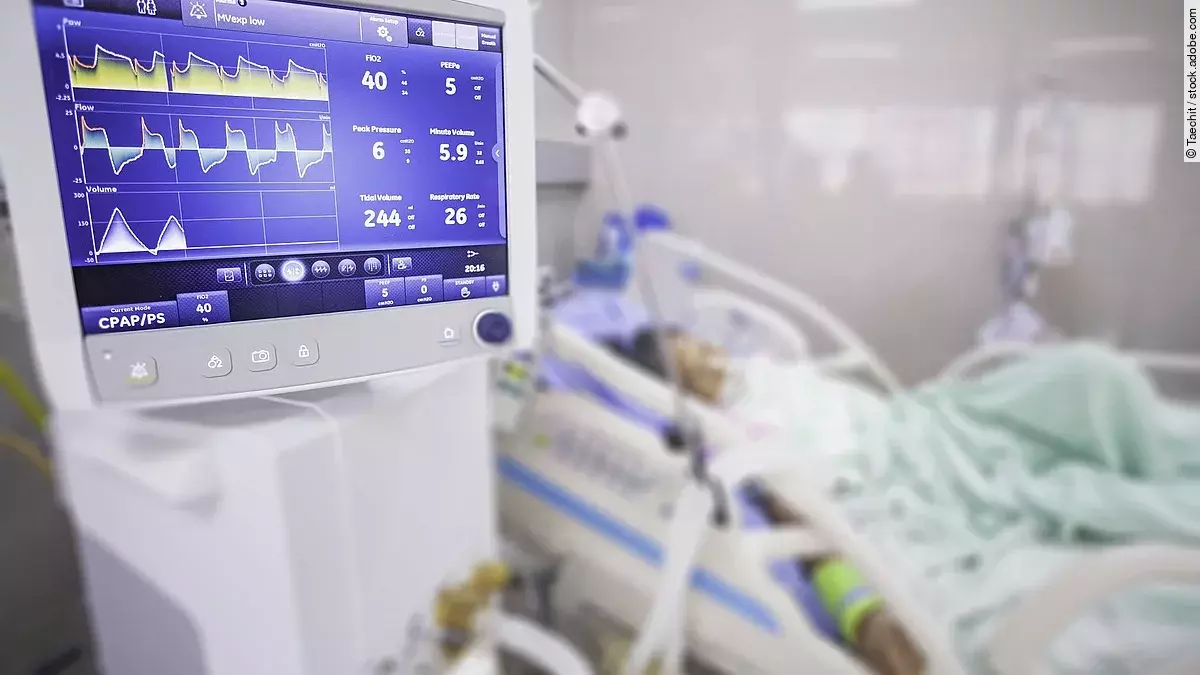
Die Symptome der Erkrankung sind vielseitig und hängen davon ab, welche Bakterien sie auslösen und wo sie sich eingenistet haben. Verschiedene Geräte auf den Intensivstationen erheben permanent Daten der Patienten – circa 200 Vitalparameter wie Körpertemperatur oder Blutwerte werden alle vier Stunden gemessen. Eine wichtige Grundlage für die künstliche Intelligenz, die all diese Parameter zusammenführt und Behandlungsvorschläge errechnet, etwa das Verabreichen bestimmter Medikamente. Im Wesentlichen seien das zwei Medikamente, um den Kreislauf zu stabilisieren.
Mit Erfolg – denn die Analysen zeigen, dass die Fähigkeiten der KI den Menschen übertreffen. In Bezug auf die 90-Tage-Mortalität konnte die Heilungsquote um drei Prozent auf 88 Prozent gesteigert werden. „Der Lernalgorithmus zieht mehr Merkmale in Betracht und das ist sicher einer der Gründe, aus dem die Maschine Vorteile ziehen und bessere Regeln lernen kann“, erklärt Heitzinger, der auch Co-Director des Center for Artificial Intelligence and Machine Learning (CAIML) der TU Wien ist.
Die KI blickt in die Zukunft
Doch wie lernt die KI überhaupt? Maschinelles Lernen besteht im Grunde aus drei Teilgebieten: Supervised Learning, Unsupervised Learning und Reinforcement Learning. „Das erste und wichtigste Ziel im Reinforcement Learning ist, dass wir optimale Behandlungsstrategien berechnen“, sagt Heitzinger.
Im Gegensatz zu Supervised beziehungsweise Unsupervised Learning sind die Prozesse dabei zeitabhängig. Es ist auch eine Erkennung, ähnlich wie beim Supervised Learning, bei dem es beispielsweise um das Erkennen von Auffälligkeiten in der Bildgebung geht. Diese Erkennung findet aber in jedem Zeitschritt statt, da die Daten des betroffenen Patienten regelmäßig neu erhoben werden. „Die Schwierigkeit im Reinforcement Learning ist, dass wir in die Zukunft blicken müssen“, so der Mathematiker. Es geht nicht nur um eine „ja“- oder „nein“-Entscheidung, wie bei Bildklassifizierungen, sondern man muss beachten, dass Aktionen, die zum aktuellen Zeitpunkt gesetzt werden, Auswirkungen auf einen viel späteren Zeitpunkt haben werden.
Maschinelles Lernen
- Supervised Learning: Dem Algorithmus wird ein Datensatz, bei dem die Zielvariable bekannt ist, vorgelegt. Er erlernt Zusammenhänge und Abhängigkeiten in den Daten, die die Zielvariable erklären. Nach diesem Prinzip funktionieren künstliche Intelligenzen aus der Bildgebung.
- Unsupervised Learning: Bei dieser Methode lernt der Algorithmus selbstständig Muster und Zusammenhänge in Daten zu erkennen. Patienten können dadurch zum Beispiel in Gruppen, die sich ähneln, eingeteilt werden.
- Reinforcement Learning: Bedeutet „bestärkendes Lernen“. Dabei erhält ein Agent Belohnungen, wenn er seine Aufgabe erfüllt. Er erlent eigenständig eine Strategie, um den Erwartungswert der Summe aller zukünftigen Belohnungen zu maximieren, er muss also weit in die Zukunft blicken. Dabei hat er gelernt, in welcher Situation welche Aktion am besten ist.
Eine gute Aktion am Anfang könne über das Überleben 20 oder 30 Zeitschritte später entscheiden – ebenso kann ein Fehler zeitversetzt fatale Auswirkungen haben. Die Belohnung, die Bestandteil des Reinforcement Learnings ist, wird am Ende einer Episode vergeben – auf diesem Prinzip basiert beispielsweise auch ChatGPT. Die Belohnung ist in dem Fall, ob die Antwort hilfreich war oder nicht. Im Fall der Sepsis entspricht eine Episode dem Aufenthalt eines Patienten auf der Intensivstation, was etwa zwei bis drei Tage sind. Entscheidend sind dabei die Überlebensraten nach 28 beziehungsweise 90 Tagen, die erhoben werden.
Im Prinzip kann man unseren Ansatz für jede Krankheit nutzen.
Die Daten der rund 10 000 Patienten stammen aus mehreren großen Datenbanken, unter anderem der MIMIC-Datenbank des Massachusetts Institute of Technology (MIT). Aus diesen wurden die optimalen Behandlungsstrategien gelernt. „Wir sehen, was in der Vergangenheit passiert ist, wenn Medikament ‚X‘ verabreicht wurde und können daraus optimale Strategien ausrechnen“, sagt Heitzinger. Unter gewissen – technischen – Voraussetzungen könne man zeigen, dass die Algorithmen tatsächlich optimale Strategien ausrechnen.
Aktuell wird noch viel Zeit in die Evaluierung investiert – das nächste Ziel ist die Zulassungsstudie. Ist dieses Ziel erreicht, kann die KI auch im Klinikalltag genutzt werden. Doch die Arbeit geht weiter. So sollen die Algorithmen dahingehend verbessert werden, dass sie schneller lernen. Eine weitere Aufgabe sieht Heitzinger darin, mehr Datenbanken verfügbar zu machen. Gerade in der Intensivmedizin könnten die Daten gut genutzt werden, oder auch bei Operationen und für weitere Anwendungen. Etwa, wenn der Blutdruck unkontrolliert abfällt. Zwar kündigt sich das meistens an, wenn man es aber nur wenige Minuten früher zuverlässig erkennt, wäre es ein großer Vorteil für den Patienten. „Im Prinzip kann man unseren Ansatz für jede Krankheit nutzen. Es liegt eigentlich nur an der Verfügbarkeit von Datensätzen, die groß genug sind“, so sein Fazit.








Derzeit sind noch keine Kommentare vorhanden. Schreiben Sie den ersten Kommentar!
Jetzt einloggen